牛蒡苷(arctiin)及牛蒡苷元(arctigenin)的藥理研究新知
民國100年10月號
牛蒡苷 (arctiin) 及牛蒡苷元 (arctigenin) 的藥理研究新知
中藥牛蒡子為菊科 (Compositae) 植物牛蒡 (Arctium lappa LINN.) 之乾燥成熟果實,味辛、苦,性寒,歸肺、胃經,能疏散風熱、宜肺透疹、解毒利咽 [1],原名「惡實」,始載於《名醫別錄》,列為中品,舉凡《本草圖經》、《本草衍義》、《本草綱目》、《證類本草》、《大觀本草》、《本草品匯精要》等典籍皆有記載 [2],又稱大力子、牛子、鼠黏子等,主產於中國東北及浙江省 [3]。
牛蒡子主要成分為木質酚素類 (lignans) 化合物,包括:牛蒡苷 (arctiin)、牛蒡苷元 (arctigenin)、羅漢松脂素 (matairesinol)、牛蒡酚 (lappaol) A、B、C、D、E、F、H、異牛蒡酚 (isolappaol)、新牛蒡素 A、B (neoarctins A, B)、牛蒡子素 (arctignans) A、B、C、D、E、揮發油、少量生物鹼、固醇、蛋白質等 [4-6]。牛蒡苷元為牛蒡苷分解而得到的產物 [7],為牛蒡子的主要活性成份,在牛蒡子中含量約占 0.13~1.04%,而牛蒡苷約占 2.64~8.02% [8]。
牛蒡子應用於傳統醫學的歷史悠久,因此科學家們也對其藥理活性成份進行研究,目前由文獻得知牛蒡苷有:抗癌 [9-13]、生物活性轉換 [14]、抗發炎 [15]、抗病毒 [16];牛蒡苷元有:抗病毒 [16-21]、生物活性轉換 [22]、免疫調控 [23, 24]、清除自由基 [25]、神經保護 [21, 26]、化學防護 [27, 28]、肝臟保護 [29]、抗癌 [30-35]、解熱 [36]、抗發炎 [21, 37-39] 等藥理活性。
關於牛蒡苷及牛蒡苷元的藥理作用研究已持續多年,近年來更有許多文獻對其藥理機制作深入的探討,茲就 2011 年最近的研究成果作扼要地摘述,以供現在未來研究之參考:
1. 改善記憶力衰退:
牛蒡子在傳統草藥醫學中,常應用於治療發炎性疾病,因此 Lee 等人探討了牛蒡苷元對 scopolamine 誘發小鼠記憶力衰退的影響,結果發現其主要成份牛蒡苷及牛蒡苷元皆能抑制乙醯膽鹼酯酶 (acetylcholine esterase, AChE) 的活性,而牛蒡苷元的抑制效果較牛蒡苷更佳。在被動迴避試驗 (passive avoidance test) 中,與口服 10 mg/kg 的 tacrine 小鼠相較之下,口服 30 mg/kg 與 60 mg/kg 牛蒡苷元的小鼠記憶力衰退分別改善了 62% 與 73%;在 Y 迷宮與 Morris 水迷宮試驗 (Y-maze and Morris water maze tests) 中,小鼠口服牛蒡苷元亦能顯著改善記憶力的衰退。
此外,牛蒡苷元也降低了 scopolamine 誘發小鼠腦部下視丘升高的腫瘤壞死因子 (tumor necrosis factor-α,TNF-α) 的濃度。Lee 等人由上述實驗結果,推測牛蒡苷元可能藉由抑制 AChE 活性及增高的 TNF-α 濃度而達到改善記憶力衰退的作用 [40]。
2. 抗發炎:
過去研究發現牛蒡苷元具有抗發炎作用,但科學家對其機制尚未有完整透徹的研究。因此 Kou 等人研究了牛蒡苷元對脂多醣 (lipopolysaccharide, LPS) 誘發 RAW264.7 巨噬細胞生成發炎前驅介質 (proinflammatory mediators) 以及其相關藥理機制的影響,實驗結果發現牛蒡苷元能藉由其抗氧化活性而抑制與活性氧 (reactive oxygen species, ROS) 有關的轉錄訊息傳遞子與活化子 (signal transducers and activators of transcription, STAT) 之訊息傳遞,同時也能顯著減少 LPS 所致 RAW264.7 巨噬細胞 STAT1、STAT3 與 Janus 激酶 (Janus kinase 2, JAK2) 的磷酸化,導致 STAT1 與 STAT3 無法轉位 (translocation) 至細胞核內,進而抑制誘發型一氧化氮合成酶 (inducible nitric oxide synthase, iNOS) 以及具有 STAT 結合序列促進子 (promoters) 之發炎相關基因 IL-1β、IL-6 與 MCP-1 的表現。
另一方面,牛蒡苷元在較高濃度 (50 μM) 對環氧酶 (cyclooxygenase-2, COX-2) 的表現有輕微的抑制作用。綜上實驗結果,Kou 等人推論牛蒡苷元可能藉由阻斷受 LPS 刺激的 RAW264.7 巨噬細胞 JAK-STAT 訊息傳遞路徑,而能抑制 iNOS 表現,達到抗發炎的作用 [41]。
3. 抗氧化及抗增殖:
Predes 等人評估了牛蒡根部萃取物總酚類成份、DPPH 自由基清除活性以及體外抗增殖實驗,分別以高溫及室溫的二氯甲烷、乙醇與水萃取牛蒡根部得到萃取物,以 DPPH 自由基清除實驗觀察水乙醇萃取物與總水萃取物自由基清除能力、Folin-Ciocalteau 法檢測總酚類成份、人類癌細胞株評估體外抗增殖活性以及高解析電噴灑離子化質譜儀 (high-resolution electrospray ionization mass spectroscopy, HRESI-MS) 分析水乙醇萃取物。實驗結果發現:水乙醇萃取物有較佳的自由基清除能力,酚類成份以二氯甲烷經 Soxhlet 及浸漬萃取法之萃取物以及水乙醇萃取物含量較多,HRESI-MS 分析水乙醇萃取物含有牛蒡苷元、槲皮素 (quercetin)、綠原酸 (chlorogenic acid) 以及咖啡酸 (caffeic acid) 等化合物;而唯一具有抗癌細胞株生長作用的萃取物為二氯甲烷萃取物,特別是對 K562、MCF-7 與 786-0 等細胞株有顯著的抑制作用。Predes 等人由上述實驗結果得到推論:水乙醇萃取物具有最強的自由基清除能力,而以 Soxhlet 萃取法能得到最多的酚類成份,二氯甲烷萃取物對 K562、MCF-7 與 786-0 等人類癌細胞株有顯著的抗增殖作用 [42]。
4. 免疫調控:
衛生福利部國家中醫藥研究所蔡維人研究員等人研究牛蒡苷元對於抗 CD3/CD28 抗體所致人類 T 淋巴細胞增殖及細胞激素基因表現的影響。以酵素免疫分析法及氚化胸腺嘧啶 (tritiated thymidine) 吸收法觀察細胞增殖的情形,反轉錄-聚合酶鍊反應 (reverse transcription-polymerase chain reaction) 分析細胞激素生成及基因表現的情形。
實驗結果發現:牛蒡苷元能抑制抗 CD3/CD28 抗體所致人類 T 淋巴細胞增殖,而細胞存活率實驗顯示牛蒡苷元抑制其增殖的作用與直接進行細胞毒殺無關。另一方面,牛蒡苷元能濃度相關性地抑制抗 CD3/CD28 抗體所致人類 T 淋巴細胞介白素-2 (interleukin-2, IL-2) 與干擾素-γ (interferon-γ, IFN-γ) 的生成,並能減少此二種細胞激素的基因表現。
在報導基因 (reporter gene) 分析實驗中,牛蒡苷元能減少活化 T 細胞核因子 (nuclear factor of activated T cells, NF-AT) 為媒介的報導基因表現。因此本所蔡維人研究員等人,歸納上述實驗結果得到結論為:牛蒡苷元能抑制 T 淋巴細胞增殖,並能藉由抑制 NF-AT 途徑而減少 IL-2 與 IFN-γ 的基因與蛋白質表現 [43]。
5. 抗癌:
牛蒡苷元在牛蒡、水母雪蓮 (Saussurea medusa)、日本榧 (Torreya nucifera) 以及槭葉牽牛 (Ipomea cairica) 等植物中皆可分離得到,過去研究顯示其抗發炎作用是藉由抑制核因子-κB (nuclear factor-kappaB, NF-κB) 而達到的,但在 JAK-STAT3 訊息路徑中所扮演角色之相關研究較少。因此 Yao 等人研究了牛蒡苷元對 STAT3 訊息路徑的影響,並評估了牛蒡苷元抑制 STAT3 的活性是否能增加癌細胞對化療藥物順鉑 (cisplatin) 的敏感度。
實驗結果顯示牛蒡苷元能顯著抑制癌細胞活化的及 IL-6 誘導的 STAT3 磷酸化及細胞核轉位,藉由抑制 Src, JAK1 與 JAK2 而能抑制STAT3 酪胺酸磷酸化,並藉由抑制細胞外訊息調控激酶 (extracellular signal regulated kinase, ERK) 活化而能抑制 STAT3 絲胺酸磷酸化。過氧化釩酸鹽 (pervanadate) 能逆轉牛蒡苷元抑制 STAT3 活化的情形,這可能與蛋白酪胺酸磷酸酶 (protein tyrosine phosphatase, PTP) 有關,因為牛蒡苷元能顯著誘導具有 Src 同源區 2 的 domain 的蛋白酪胺酸磷酸酶 (Src homology 2-domain-containing protein tyrosine phosphatase, SHP-2) 的表現。
另一方面,STAT3 的活化程度與癌細胞抵抗順鉑誘導細胞凋亡的能力有密切關聯性,而牛蒡苷元能顯著促進順鉑誘導癌細胞死亡,顯示牛蒡苷元可能藉由抑制 STAT3 的活化而增加癌細胞對順鉑的敏感度。Yao 等人由上述實驗觀察推論:牛蒡苷元為一種天然抗癌劑,未來若能於臨床結合順鉑化療癌症可謂是非常具有發展潛力的治療方法 [44]。
胃癌在全球的致死率僅次於肺癌,但迄今有關牛蒡苷元對抗胃癌分子機制的研究仍不是非常透徹。因此 Jeong 等人探討了牛蒡苷元對人類胃癌細胞株 SNU-1 與 AGS 的生物效用,以 MTT 法觀察牛蒡苷元對 SNU-1 與 AGS 細胞增殖的影響,結果與空白對照組相較,牛蒡苷元能顯著抑制 SNU-1 與 AGS 細胞的增殖且改變了 Bcl-2/Bax 表現的比率,顯示抑制作用可能與細胞凋亡有關。此外,牛蒡苷元能調控細胞週期調節蛋白 Rb、週期素 (cyclin) D1、E、CDK4、CDK2、p21Waf1/Cip1 與 p15 INK4b,而能阻斷細胞週期的 G1 至 S 期。Jeong 等人由以上實驗結果得知牛蒡苷元對 SNU-1 與 AGS 胃癌細胞具有抗增殖作用,並推論牛蒡苷元未來有可能發展成為有用的抗癌化學防護劑或化療藥 [45]。
過去有研究指出牛蒡苷元能阻斷 SW480 人類大腸癌細胞與 AGS 人類胃癌細胞週期的 G2/M 期,而 Kang 等人研究了牛蒡苷元對 SW480 細胞本體及細胞核體積大小的影響。結果以螢光顯微鏡觀察發現牛蒡苷元能使 SW480 細胞本體及細胞核變大,呈現出巨型細胞核;細胞經碘化丙啶 (propidium iodide) 染色後,以光散射及加寬螢光流式細胞儀分析細胞本體及細胞核大小,結果牛蒡苷元使 SW480 細胞本體的參考數值 FSC-H 與細胞核的參考數值 FL2-W 顯著增加,FSC-H 與 FL2-W 之平均值各為 572.6 與 275.1,而空白對照組的平均值則各為 482.0 與 220.7。Kang 等人由實驗結果推論以上述方法能協助檢視植化素誘導的細胞本體及細胞核變大的情形,對抗癌藥物而言是有用的研究 [46]。
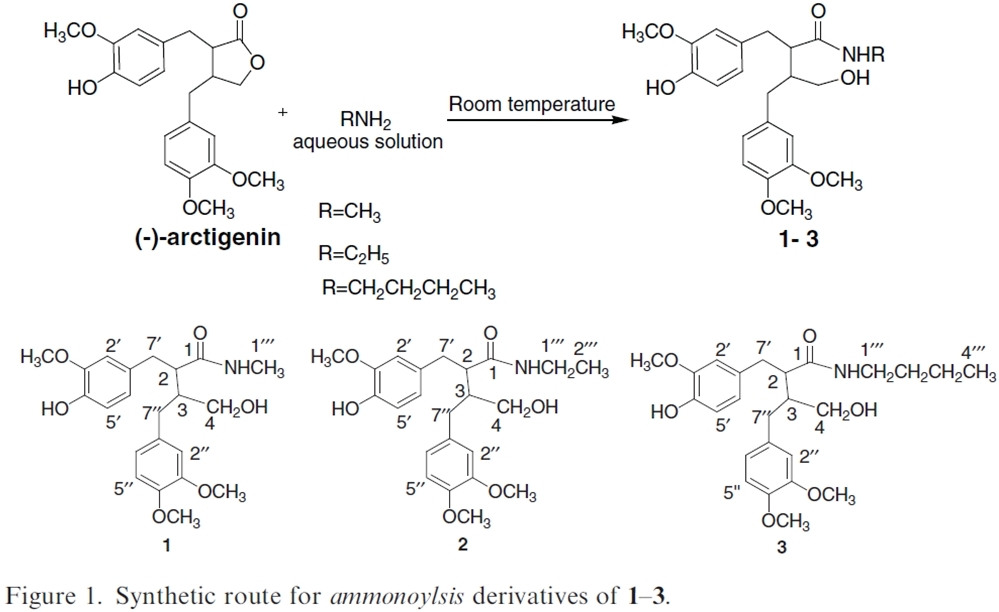
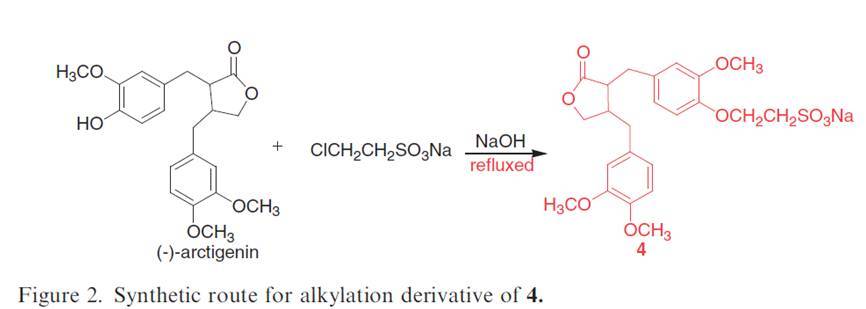
牛蒡子天然 dibenzylbutyrolactone 型木質內酯 (lignanolide) 成份牛蒡苷元具有顯著的抗癌活性,Chen 等人合成了四種新的牛蒡苷元衍生物 1-4:1-3 為牛蒡苷元經氨解 (ammonoylsis) 反應所得到的衍生物,而 4 則為牛蒡苷元與 2-氯-乙基磺酸鈉 (2-chloro-ethylsulfonate sodium) 經烷化 (alkylation) 反應所得到的衍生物(如下圖所示),並以核磁共振光譜儀 (NMR) 對 1-4 進行結構鑑定,同時也在人類大腸癌 HCT116、人類胃癌 MGC-803、人類肺癌 NCI-H460、人類星狀神經膠細胞癌 U251 以及人類胰臟癌 PANC-1 等五種癌細胞株中,檢測了它們與牛蒡苷元的抗癌活性。結果 1 與 2 有微弱的細胞毒殺力,3 與 4 有中度的細胞毒殺力,但 1-4 的細胞毒殺力皆較牛蒡苷元弱。Chen 等人由上述實驗結果推測內酯環狀結構與酚羥基結構可能是影響抗癌活性的關鍵因素 [47]。
6. 提高小鼠疲勞耐受度:
缺乏運動是第二型糖尿病及其他代謝相關疾病的危險因子之一,而耐力運動訓練 (endurance exercise training) 能促進脂肪代謝、增加胰島素敏感度並改善肥胖。單磷酸腺苷活化蛋白激酶 (AMP-activated protein kinase, AMPK) 在調控人體熱量恆定性 (homeostasis) 的過程中如同熱量感測器,它的活化能改善葡萄糖吸收、促進粒線體生物合成並能增加糖解作用。
最近的研究指出 AMPK 的活化能促進不運動情況下的耐力,但有關牛蒡苷元對 AMPK 影響的研究並不多,因此 Tang 等人研究了牛蒡苷元對 AMPK 的作用機制,結果發現牛蒡苷元能顯著增加 H9C2 心肌細胞與 C2C12 肌纖維細胞 AMPK 的磷酸化及其下游訊息路徑的活化,主要機制為經由攜鈣素相關蛋白激酶 (calmodulin-dependent protein-kinase kinase, CaMKK) 以及絲胺酸/蘇胺酸激酶 (serine/threonine kinase 1, LKB1) 之相關訊息傳遞路徑活化所致。
活體實驗中,牛蒡苷元能延長小鼠在其專用平板式跑步機上跑步時疲勞出現的時間及增加可跑的距離,改善疲勞耐受度,同時也能促進小鼠肌肉組織中粒線體的生物合成與脂肪酸氧化相關基因的表現。Tang 等人由上述實驗結果推測牛蒡苷元可能具有類似運動訓練後促進代謝的藥理作用,未來也許有機會研發成為治療代謝性疾病的藥物 [48]。
參考文獻
1. 國家藥典委員會,《中華人民共和國藥典》,化學工業出版社,pp.48-49,2005。
2. 許亮、竇德強、康廷國,牛蒡子本草考證及道地變遷,現代中藥研究與實踐,24:24-26,2010。
3. 高雪敏,中藥學,中國中醫藥出版社,北京,pp.76-77,2002。
4. 李燕、孫敬勇、武海艷、仲英,牛蒡子化學成分及藥理作用研究進展,齊魯藥事,28:738-740,2009。
5. Wang, H.Y., Yan, J.S. Neoarctin A from Arctium lappa L.. Chin. Chem. Lett., 6:217-220, 1995.
6. Umehara, K., Sugawa, A., Kuroyanagi, M., Ueno, A., Taki, T. Studies on differentiation-inducers from Arctium Fructus. Chem. Pharm. Bull., 41:1774-1779, 1993.
7. 胡英杰、樊蘊華、肖敏勛、周娟、盧元媛、楊子峰、朱宇同,蝸牛酶水解牛蒡子苷製備苷元的研究,廣州中醫藥大學學報, 21:473-475、481,2004。
8. 米靖宇、汪志超、宋純清,高效液相色譜法測定不同採購地牛蒡子中牛蒡子苷和苷元的含量,時珍國醫國藥,15:737-739,2004。
9. Kato, T., Hirose, M., Takahashi, S., Hasegawa, R., Kohno, T., Nishibe, S., Kato, K., Shirai, T. Effects of the lignan, arctiin, on 17-beta ethinyl estradiol promotion of preneoplastic liver cell foci development in rats. Anticancer Res., 18:1053-1057, 1998.
10. Hirose, M., Yamaguchi, T., Lin, C., Kimoto, N., Futakuchi, M., Kono, T., Nishibe, S., Shirai, T. Effects of arctiin on PhIP-induced mammary, colon and pancreatic carcinogenesis in female Sprague-Dawley rats and MeIQx-induced hepatocarcinogenesis in male F344 rats. Cancer Lett., 155:79-88, 2000.
11. Huang, D.M., Guh, J.H., Chueh, S.C., Teng, C.M. Modulation of anti-adhesion molecule MUC-1 is associated with arctiin-induced growth inhibition in PC-3 cells. Prostate, 59:260-267, 2004.
12. Hasumura, M., Ueda, M., Onose, J., Imai, T., Hirose, M. Lack of a significant effect of arctiin on development of 7,12-dimethylbenz(a)anthracene-induced mammary tumors in ovariectomized Sprague-Dawley rats. Nutr. Cancer, 57:201-208, 2007.
13. Matsuzaki, Y., Koyama, M., Hitomi, T., Yokota, T., Kawanaka, M., Nishikawa, A., Germain, D., Sakai, T. Arctiin induces cell growth inhibition through the down-regulation of cyclin D1 expression. Oncol. Rep., 19:721-727, 2008.
14. Xie, L.H., Ahn, E.M., Akao, T., Abdel-Hafez, A.A., Nakamura, N., Hattori, M. Transformation of arctiin to estrogenic and antiestrogenic substances by human intestinal bacteria. Chem. Pharm. Bull., 51:378-384, 2003.
15. Wu, J.G., Wu, J.Z., Sun, L.N., Han, T., Du, J., Ye, Q., Zhang, H., Zhang, Y.G. Ameliorative effects of arctiin from Arctium lappa on experimental glomerulonephritis in rats. Phytomedicine, 16:1033-1041, 2009.
16. Hayashi, K., Narutaki, K., Nagaoka, Y., Hayashi, T., Uesato, S. Therapeutic effect of arctiin and arctigenin in immunocompetent and immunocompromised mice infected with influenza A virus. Biol. Pharm. Bull., 33:1199-1205, 2010.
17. Schröder, H.C., Merz, H., Steffen, R., Müller, W.E., Sarin, P.S., Trumm, S., Schulz, J., Eich, E. Differential in vitro anti-HIV activity of natural lignans. Z. Naturforsch. C, 45:1215-1221, 1990.
18. Eich, E., Pertz, H., Kaloga, M., Schulz, J., Fesen, M.R., Mazumder, A., Pommier, Y. (-)-Arctigenin as a lead structure for inhibitors of human immunodeficiency virus type-1 integrase. J. Med. Chem., 39:86-95, 1996.
19. Vlietinck, A.J., De Bruyne, T., Apers, S., Pieters, L.A. Plant-derived leading compounds for chemotherapy of human immunodeficiency virus (HIV) infection. Planta Med., 64:97-109, 1998.
20. 楊子峰、劉妮、黃碧松、王艷芳、胡英杰、朱宇同,牛蒡子甙元體內抗甲1型流感病毒作用的研究,中藥材,28:1012-1014,2005。
21. Swarup, V., Ghosh, J., Mishra, M.K., Basu, A. Novel strategy for treatment of Japanese encephalitis using arctigenin, a plant lignan. J. Antimicrob. Chemother., 61:679-688, 2008.
22. Kasper, R., Gansser, D., Doehmer, J. Biotransformation of the naturally occurring lignan (-)-arctigenin in mammalian cell lines genetically engineered for expression of single cytochrome P450 isoforms. Planta Med., 60:441-444, 1994.
23. Cho, J.Y., Kim, A.R., Yoo, E.S., Baik, K.U., Park, M.H. Immunomodulatory effect of arctigenin, a lignan compound, on tumour necrosis factor-alpha and nitric oxide production, and lymphocyte proliferation. J. Pharm. Pharmacol., 51:1267-1273, 1999.
24. Cho, M.K., Jang, Y.P., Kim, Y.C., Kim, S.G. Arctigenin, a phenylpropanoid dibenzylbutyrolactone lignan, inhibits MAP kinases and AP-1 activation via potent MKK inhibition: the role in TNF-alpha inhibition. Int. Immunopharmacol., 4:1419-1429, 2004.
25. Sibi, M.P., Liu, P., Ji, J., Hajra, S., Chen, J.X. Free-radical-mediated conjugate additions. Enantioselective synthesis of butyrolactone natural products: (-)-enterolactone, (-)-arctigenin, (-)-isoarctigenin, (-)-nephrosteranic acid, and (-)-roccellaric acid. J. Org. Chem., 67:1738-1745, 2002.
26. Jang, Y.P., Kim, S.R., Choi, Y.H., Kim, J., Kim, S.G., Markelonis, G.J., Oh, T.H., Kim, Y.C. Arctigenin protects cultured cortical neurons from glutamate-induced neurodegeneration by binding to kainate receptor. J. Neurosci. Res., 68:233-240, 2002.
27. Hausott, B., Greger, H., Marian, B. Naturally occurring lignans efficiently induce apoptosis in colorectal tumor cells. J. Cancer Res. Clin. Oncol., 129:569-576, 2003.
28. Kang, K., Lee, H.J., Kim, C.Y., Lee, S.B., Tunsag, J., Batsuren, D., Nho, C.W. The chemopreventive effects of Saussurea salicifolia through induction of apoptosis and phase II detoxification enzyme. Biol. Pharm. Bull., 30:2352-2359, 2007.
29. Kim, S.H., Jang, Y.P., Sung, S.H., Kim, C.J., Kim, J.W., Kim, Y.C. Hepatoprotective dibenzylbutyrolactone lignans of Torreya nucifera against CCl4-induced toxicity in primary cultured rat hepatocytes. Biol. Pharm. Bull., 26:1202-1205, 2003.
30. Awale, S., Lu, J., Kalauni, S.K., Kurashima, Y., Tezuka, Y., Kadota, S., Esumi, H. Identification of arctigenin as an antitumor agent having the ability to eliminate the tolerance of cancer cells to nutrient starvation. Cancer Res., 66:1751-1757, 2006.
31. Matsumoto, T., Hosono-Nishiyama, K., Yamada, H. Antiproliferative and apoptotic effects of butyrolactone lignans from Arctium lappa on leukemic cells. Planta Med., 72:276-278, 2006.
32. 王潞、趙烽、劉珂,牛蒡子苷元誘導人白血病細胞凋亡的作用及機制,藥學學報,43:542-547,2008。
33. Kim, J.Y., Hwang, J.H., Cha, M.R., Yoon, M.Y., Son, E.S., Tomida, A., Ko, B., Song, S.W., Shin-ya, K., Hwang, Y.I., Park, H.R. Arctigenin blocks the unfolded protein response and shows therapeutic antitumor activity. J. Cell. Physiol., 224:33-40, 2010.
34. Yoo, J.H., Lee, H.J., Kang, K., Jho, E.H., Kim, C.Y., Baturen, D., Tunsag, J., Nho, C.W. Lignans inhibit cell growth via regulation of Wnt/beta-catenin signaling. Food Chem. Toxicol., 48:2247-2252, 2010.
35. Sun, S., Wang, X., Wang, C., Nawaz, A., Wei, W., Li, J., Wang, L., Yu, D.H. Arctigenin suppresses unfolded protein response and sensitizes glucose deprivation-mediated cytotoxicity of cancer cells. Planta Med., 77:141-145, 2011.
36. Ishihara, K., Yamagishi, N., Saito, Y., Takasaki, M., Konoshima, T., Hatayama, T. Arctigenin from Fructus Arctii is a novel suppressor of heat shock response in mammalian cells. Cell Stress Chaperones, 11:154-161, 2006.
37. Kang, H.S., Lee, J.Y., Kim, C.J. Anti-inflammatory activity of arctigenin from Forsythiae Fructus. J. Ethnopharmacol., 116:305-312, 2008.
38. Zhao, F., Wang, L., Liu, K. In vitro anti-inflammatory effects of arctigenin, a lignan from Arctium lappa L., through inhibition on iNOS pathway. J. Ethnopharmacol., 122:457-462, 2009.
39. Lee, J.Y., Kim, C.J. Arctigenin, a phenylpropanoid dibenzylbutyrolactone lignan, inhibits type I-IV allergic inflammation and pro-inflammatory enzymes. Arch. Pharm. Res., 33:947-957, 2010.
40. Lee, I.A., Joh, E.H., Kim, D.H. Arctigenin isolated from the seeds of Arctium lappa ameliorates memory deficits in mice. Planta Med., 77:1525-1527, 2011.
41. Kou, X., Qi, S., Dai, W., Luo, L., Yin, Z. Arctigenin inhibits lipopolysaccharide-induced iNOS expression in RAW264.7 cells through suppressing JAK-STAT signal pathway. Int. Immunopharmacol., 11:1095-1102, 2011.
42. Predes, F.S., Ruiz, A.L., Carvalho, J.E., Foglio, M.A., Dolder, H. Antioxidative and in vitro antiproliferative activity of Arctium lappa root extracts. BMC Complement Altern. Med., 11:25, 2011.
43. Tsai, W.J., Chang, C.T., Wang, G.J., Lee, T.H., Chang, S.F., Lu, S.C., Kuo, Y.C. Arctigenin from Arctium lappa inhibits interleukin-2 and interferon gene expression in primary human T lymphocytes. Chin. Med., 6:12, 2011.
44. Yao, X., Zhu, F., Zhao, Z., Liu, C., Luo, L., Yin, Z. Arctigenin enhances chemosensitivity of cancer cells to cisplatin through inhibition of the STAT3 signaling pathway. J. Cell. Biochem., in press, 2011.
45. Jeong, J.B., Hong, S.C., Jeong, H.J., Koo, J.S. Arctigenin induces cell cycle arrest by blocking the phosphorylation of Rb via the modulation of cell cycle regulatory proteins in human gastric cancer cells. Int. Immunopharmacol., in press, 2011.
46. Kang, K., Lee, H.J., Yoo, J.H., Jho, E.H., Kim, C.Y., Kim, M., Nho, C.W. Cell and nuclear enlargement of SW480 cells induced by a plant lignan, arctigenin: evaluation of cellular DNA content using fluorescence microscopy and flow cytometry. DNA Cell Biol., 30:623-629, 2011.
47. Gui-Rong, C., Li-Ping, C., De-Qiang, D., Ting-Guo, K., Hong-Fu, L., Fu-Rui, L., Ning, J. Synthesis of (-)-arctigenin derivatives and their anticancer activity. Nat. Prod. Res., in press, 2011.
48. Tang, X., Zhuang, J., Chen, J., Yu, L., Hu, L., Jiang, H., Shen, X. Arctigenin efficiently enhanced sedentary mice treadmill endurance. PLoS One, 6:e24224, 2011.